
Analiza obrazów medycznych z wykorzystaniem sztucznej inteligencji szybko się rozwinęła w ostatnich latach. Teraz przeprowadzono jedno z największych do tej pory badań z wykorzystaniem wspomaganej sztuczną inteligencją analizy obrazu chłoniaka, nowotworu układu limfatycznego.
Opracowywano nowe metody wspomagania komputerowego interpretacji obrazów medycznych dla różnych schorzeń. Mogą one zmniejszyć obciążenie pracą radiologów, wydając drugą opinię lub oceniając, którzy pacjenci potrzebują leczenia najszybciej.
„Oparty na sztucznej inteligencji system komputerowy do interpretacji obrazów medycznych przyczynia się również do zwiększenia równości w opiece zdrowotnej, dając pacjentom dostęp do tej samej wiedzy i możliwość sprawdzenia ich obrazów w rozsądnym czasie, niezależnie od tego, w którym szpitalu się znajdują. Ponieważ system sztucznej inteligencji ma dostęp do znacznie większej ilości informacji, ułatwia to również leczenie chorób rzadkich, w których radiolodzy rzadko widzą obrazy”, mówi Ida Häggström, profesor nadzwyczajny na Wydziale Inżynierii Elektrycznej w Chalmers.
W ścisłej współpracy z Akademią Sahlgrenska na Uniwersytecie w Göteborgu i Szpitalem Uniwersyteckim Sahlgrenska uczestniczyła w rozwoju obrazowania medycznego w dziedzinie raka, a także w wielu innych schorzeniach, takich jak choroby układu krążenia, udar mózgu i osteoporoza.
Ida Häggström wraz z aktywnymi klinicznie naukowcami, m.in. z Memorial Sloan Kettering Cancer Center w Nowym Jorku, opracowała model komputerowy, który został niedawno zaprezentowany w czasopiśmie The Lancet Digital Health.
„Na podstawie ponad 17 000 zdjęć pobranych od ponad 5 000 pacjentów z chłoniakiem stworzyliśmy system uczący się, w którym komputery zostały przeszkolone w znajdowaniu wizualnych oznak raka w układzie limfatycznym”, mówi Häggström.
W badaniu naukowcy przeanalizowali archiwa obrazów, które sięgają ponad dziesięciu lat wstecz. Porównali ostateczną diagnozę pacjentów ze skanami pozytonowej tomografii emisyjnej (PET) i tomografii komputerowej (CT) wykonanymi przed i po leczeniu. Informacje te zostały następnie wykorzystane do wytrenowania modelu komputerowego sztucznej inteligencji w celu wykrywania oznak raka węzłów chłonnych na obrazie.
Model komputerowy opracowany przez Idę Häggström nazywa się Lars, Lymphoma Artificial Reader System i jest tak zwanym systemem głębokiego uczenia się opartym na sztucznej inteligencji. Jego działanie polega na wprowadzeniu obrazu z pozytonowej tomografii emisyjnej (PET) i analizie tego obrazu za pomocą modelu AI. Jest szkolony w znajdowaniu wzorców i cech na obrazie, aby jak najlepiej przewidzieć, czy obraz jest pozytywny, czy negatywny, tj. czy zawiera chłoniaka, czy nie.
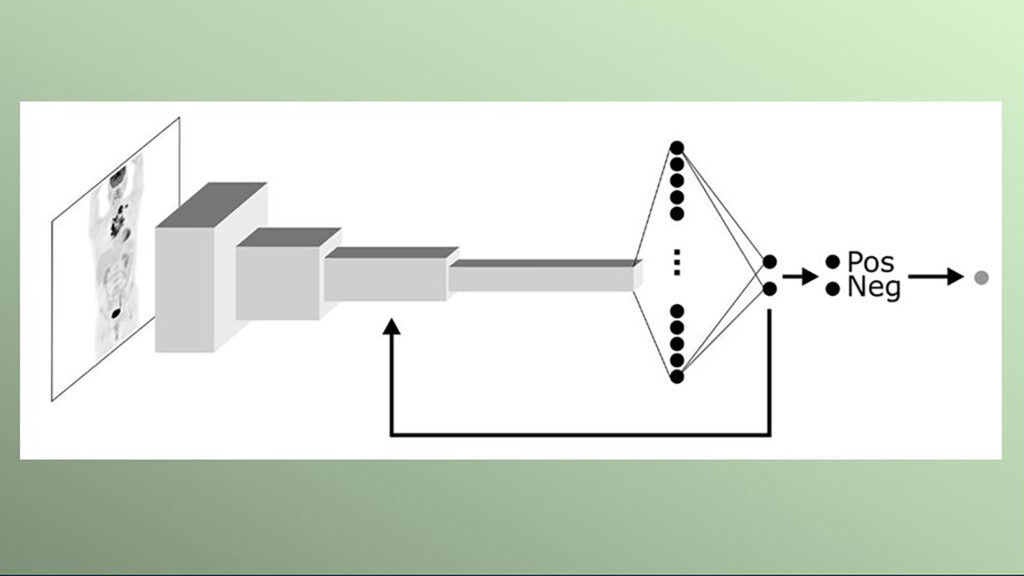
„Zastosowałam tak zwany trening nadzorowany, w którym obrazy są pokazywane modelowi komputerowemu, który następnie ocenia, czy pacjent ma chłoniaka, czy nie. Model widzi również prawdziwą diagnozę, więc jeśli ocena jest błędna, model komputerowy jest dostosowywany tak, aby stopniowo stawał się coraz lepszy w ustalaniu diagnozy”, mówi Häggström.
Co w praktyce oznacza, że model komputerowy wykorzystuje sztuczną inteligencję i głębokie uczenie do postawienia diagnozy? „Chodzi o to, że nie zaprogramowaliśmy w modelu z góry określonych instrukcji dotyczących tego, na jakie informacje na obrazie powinien patrzeć, ale pozwoliliśmy mu nauczyć się, które wzorce obrazów są ważne, aby uzyskać najlepsze możliwe prognozy.
Ida Häggström opisuje proces uczenia komputera wykrywania, w tym przypadku raka, na zdjęciach jako czasochłonny i mówi, że ukończenie badania zajęło kilka lat. Jednym z wyzwań było wyprodukowanie tak dużej ilości materiału zdjęciowego. Wyzwaniem było również dostosowanie modelu komputerowego tak, aby mógł odróżnić raka od tymczasowych zmian specyficznych dla leczenia, które można zobaczyć na obrazach po radioterapii i chemioterapii.
„W badaniu oszacowaliśmy dokładność modelu komputerowego na około dziewięćdziesiąt procent, a zwłaszcza w przypadku obrazów, które są trudne do interpretacji, może to pomóc radiologom w ich ocenach”.
Jednak nadal pozostaje wiele do zrobienia, aby zweryfikować model komputerowy, jeśli ma on być stosowany w praktyce klinicznej.
„Udostępniliśmy kod komputerowy już teraz, aby inni badacze mogli kontynuować pracę w oparciu o nasz model komputerowy, ale testy kliniczne, które należy przeprowadzić, są obszerne”, mówi Häggström.
Więcej na temat badań można dowiedzieć się TU
Źródło: materiały Uniwersytetu Technologicznego Chalmersa; zdjęcie w tekście: Uniwersytet Technologiczny Chalmers, zdjęcie zajawka: Freepik
Zostaw komentarz
You must be logged in to post a comment.